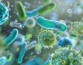
Зрительные клетки в сетчатке человека могут не только гибнуть при заболеваниях, но и выталкиваться другими клетками, обнаружили ученые из Немецкого центра нейродегенеративных исследований (DZNE) и Дрезденского центра регенеративной терапии (CRTD) при Техническом университете Дрездена. Они опробовали в лабораторных условиях и механизм блокировки «войны клеток».
Ученые использовали изготовленные в лаборатории миниатюрные человеческие сетчатки, так называемые органоиды. В новом выпуске журнала Nature Communications они сообщают о своем открытии, которое открывает путь к совершенно новым исследовательским подходам, особенно в связи с возрастной дегенерацией желтого пятна (ВМД).
«Этот принцип, известный как экструзия клеток, еще не изучался при нейродегенеративных заболеваниях», говорит возглавляющий исследовательскую группу профессор Майк Карл. ВМД является основной причиной слепоты и тяжелых нарушений зрения в Германии. Подсчитано, что четверть людей старше 60 лет страдают ВМД. Макула – это особая область в сетчатке человека, которая необходима, среди прочего, для цветного зрения с высоким разрешением. При ВМД в макуле теряются тысячи светочувствительных зрительных клеток, так называемых фоторецепторных клеток.
«Это стало отправной точкой для нашего исследовательского проекта: мы заметили, что фоторецепторы теряются, но не смогли обнаружить никакой гибели клеток в сетчатке», объясняет Майк Карл, который проводит исследования в дрезденском центре DZNE и CRTD в TU. «Половина всех фоторецепторов исчезла из органоида сетчатки в течение десяти дней, но, очевидно, они не погибли в сетчатке. Это вызвало у нас любопытство».
Исследователи из DZNE, CRTD и Центра экологических исследований им. Гельмгольца (UFZ) начали тщательный поиск причин. Джоди Розенблатт из Королевского колледжа в Лондоне первой описала экструзию живых клеток – механическое выталкивание клеток из эпителия. Вытесненные таким образом клетки умирают только последовательно. Джоди Розенблатт продемонстрировала этот механизм на простых эпителиальных клетках почки. Майк Карл и его команда показали в своей новаторской работе, что это выдавливание также может быть вызвано в гораздо более сложной сетчатке, состоящей из нескольких различных типов клеток, и приводит к нейродегенерации. Это выдавливание клеток может объяснить феномен отдаленных клеток, о которых ранее сообщалось в стареющей и пораженной сетчатке пациентов с ВМД и другими заболеваниями, но которые до сих пор подробно не изучались.
Исследователи использовали технику, которую они разработали ранее: они работали с так называемыми органоидами сетчатки – органоидной трехмерной моделью сетчатки человека, выращенной из стволовых клеток человека в лаборатории. Эти органоиды обеспечивают некоторые характеристики макулы человека. Команда обнаружила, что двух веществ, ранее описанных при различных нейродегенеративных заболеваниях, – белков HBEGF и TNF – достаточно, чтобы вызвать дегенерацию органоида сетчатки.
Во время этого процесса исследователи снимали органоиды в режиме реального времени с помощью так называемой живой визуализации, которая считается золотым стандартом для отслеживания клеток. «Мы смогли зафиксировать дегенерацию фоторецепторов путем экструзии клеток в лаборатории», говорит Майк Карл. Ученые обнаружили, что это выдавливание вызывается активацией белка PIEZO1, сенсора биомеханических сил.
То, что биомеханика может играть большую роль в дегенерации сетчатки, является новым открытием. «Неизвестно, что сетчатка является биомеханически активной тканью, такой как мышца. Было известно, что заболевания нервной системы связаны с изменением формы клеток, но до какой степени вовлечены биомеханические регуляторы, еще не изучено в деталях», говорит Карл. Благодаря органоидам он и его команда смогли наблюдать процессы в ускоренном режиме: хотя для исчезновения фоторецепторов у пациентов требуется несколько лет или даже десятилетий, такой процесс теперь можно было воспроизвести в лаборатории в всего 40 дней. На следующем этапе исследователи хотят выяснить, действует ли этот механизм у людей так же, как в органоидах. Первоначальные результаты предполагают, что это может быть тот же механизм, но доказательств еще нет.
Ученые из Дрездена также обнаружили, что фармакологические агенты могут предотвратить экструзию в экспериментальных условиях их модели. Они использовали специальный змеиный яд, чтобы заблокировать механосенсор PIEZO1 на клетках. В результате не только не происходило выброса фоторецепторов, но и предотвращались дальнейшие патологические изменения в сетчатке. «Это дает надежду на разработку будущих профилактических и терапевтических методов лечения сложных нейродегенеративных заболеваний, таких как AMD», резюмирует Майк Карл.